
2025年5月26日,深圳细胞谷团队在《Frontiers in Immunology》(中科院2区,IF 5.7)杂志发表了题为“Construction of stable packaging cell lines for large-scale industrial BaEV-enveloped retroviral vector production”的研究报告。本文详细介绍了一种BaEV包膜逆转录病毒载体的稳定包装细胞系的构建,该细胞系所制备的逆转录病毒载体更适用于NK、T等原代细胞转导。目前,我司所构建的BaEV稳转包装细胞系于2024年7月17日保藏于广东省微生物菌种保藏中心,并已授权相关专利。
深圳细胞谷提供安全性高、质量好、价格低的GMP级逆转录病毒载体及细胞治疗产品,确保细胞治疗产品的安全性和有效性,推动细胞与基因治疗行业的整体发展。


图1 论文信息(DOI:10.3389/fimmu.2025.1578660)

首先本团队利用质粒转染将逆转录病毒制备所需的结构蛋白gag-pol、BaEV包膜蛋白转进HEK293T细胞,使其稳定表达并敲除HEK293T细胞的ASCT-1/2受体,由此得到HEK293T-gag-pol-ASCT-1&2-KO细胞系。

图2 HEK293T-gag-pol细胞系的构建
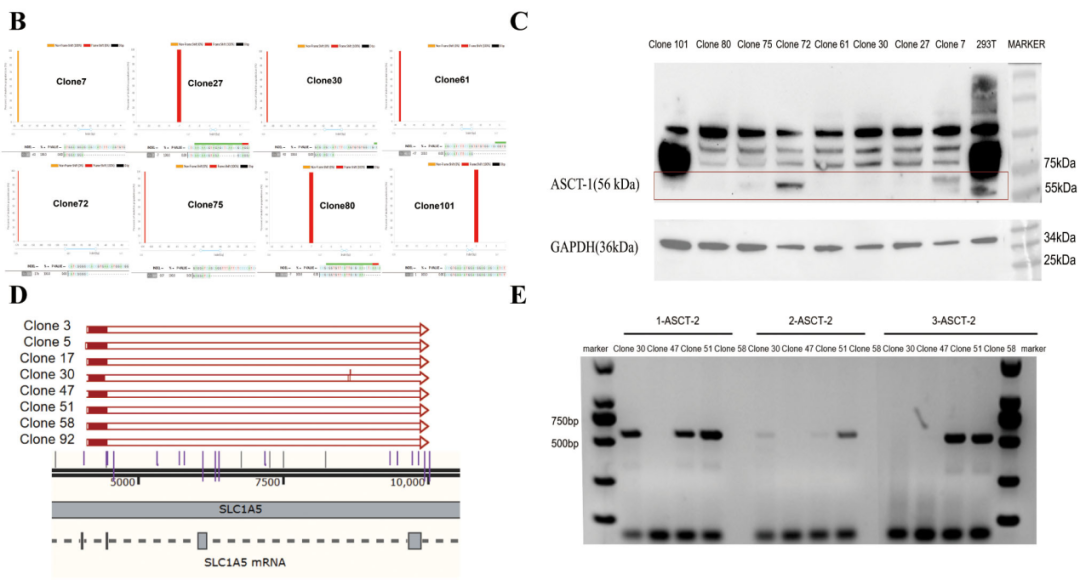
图3 HEK293T-gag-pol-ASCT-1&2-KO细胞系的构建

在此基础上,转染BaEV包膜质粒,通过抗性筛选单克隆细胞,对得到的单克隆细胞进行瞬转产毒滴度测试,筛选产毒滴度高且生长状态不受影响的单克隆细胞,即为BaEV逆转录病毒载体的稳定包装细胞株(BaEV-PackRV)。
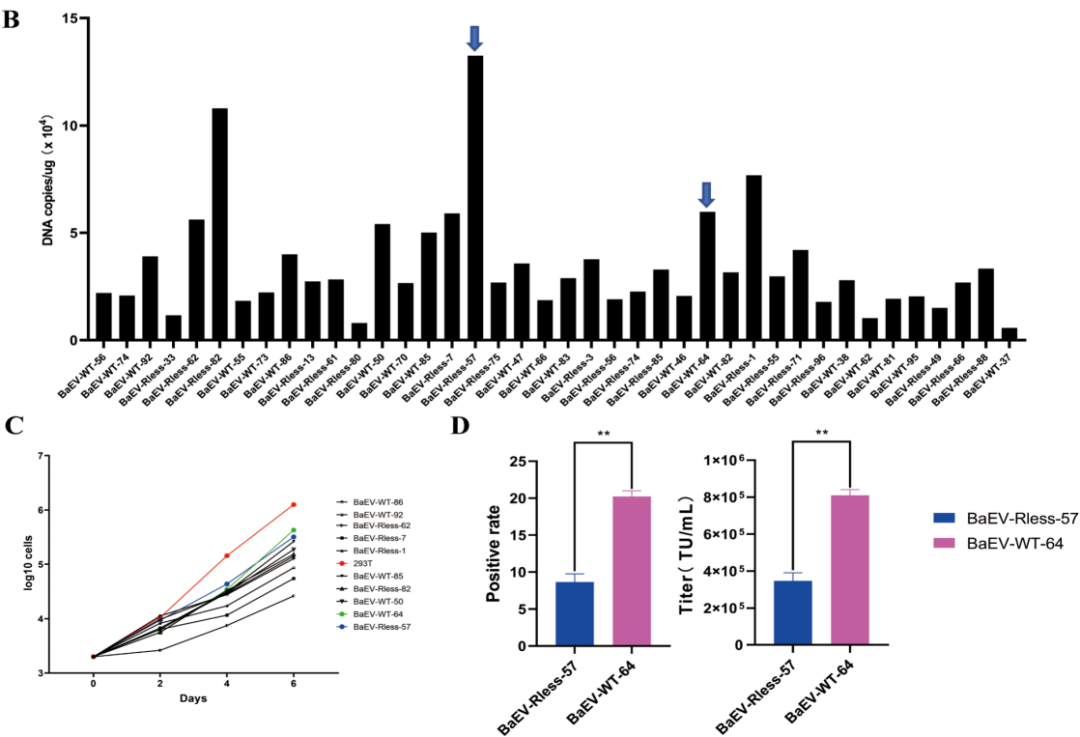
图4 HEK293T-gag-pol-ASCT-1&2-KO-BaEV细胞系的构建

基于上述所得的BaEV逆转录病毒载体包装细胞系,我们构建了BaEV-CD19 CAR-RV与传统GaLV-CD19 CAR-RV,并使用其感染原代T与NK细胞。结果表明,相较于GaLV-CD19 CAR-RV,BaEV-CD19 CAR-RV在极低滴度和低MOI下仍具有良好的原代细胞转导效率。
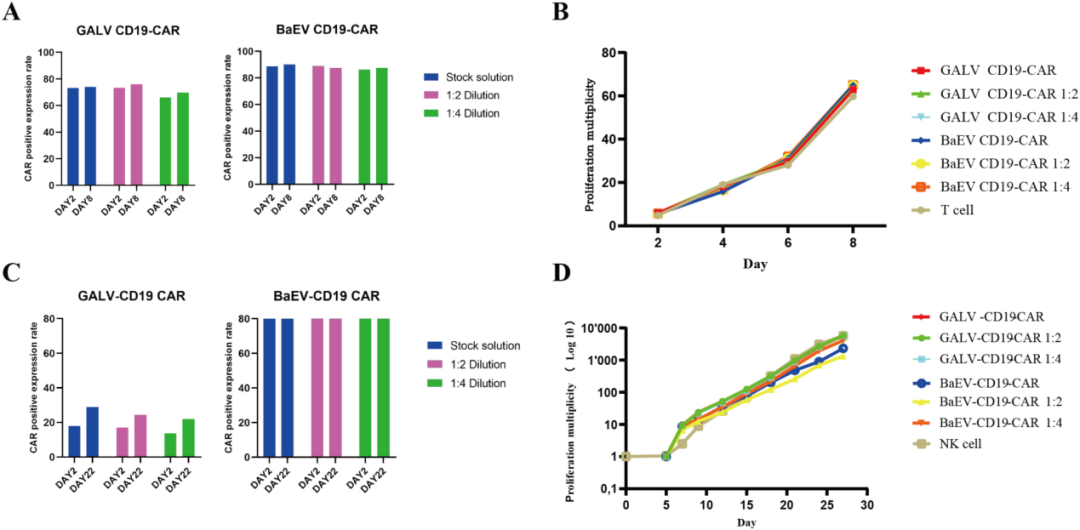
图5 BaEV/GaLV CD19-CAR RV转导人原代T细胞比较

此外,本团队测试了大规模工业生产中产生的BaEV-CD19 CAR-RV的滴度。结果表明,BaEV-CD19 CAR-RV能够在50 mL、500 mL和1 L的生产体积中维持高滴度。这表明该系统能够保障BaEV包膜逆转录病毒载体的大规模工业生产。细胞毒性试验的结果显示,由BaEV-CD19 CAR-RV制备的CAR-NK细胞表现出比由GALV-CD19 CAR-RV制备的CAR-NK细胞更强的细胞毒性。
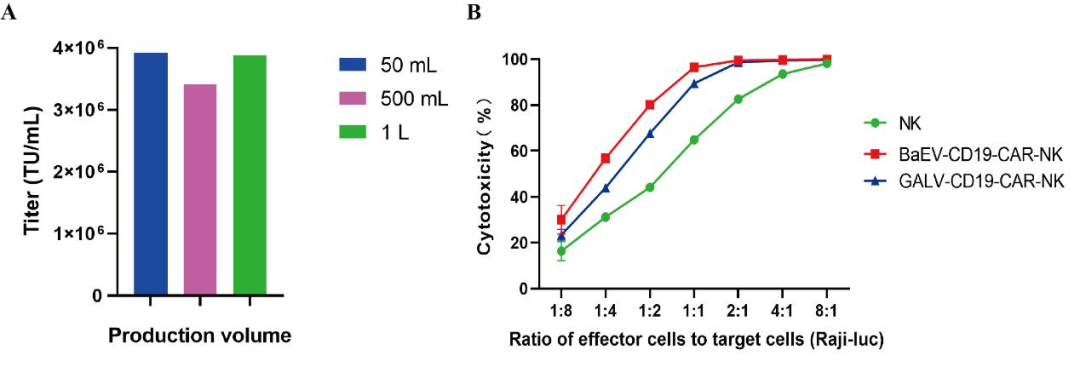
图6 大规模生产的BaEV-CD19 CAR-RV的滴度和功能验证

综上所述,本团队所研究的稳转细胞系可大批量稳定生产BaEV包膜的逆转录病毒载体,用于低成本、高质量且高效的大规模工业化制备假病毒及其在细胞治疗产品上的高效转导的应用。相较于瞬时转染的慢病毒,无需进行多质粒转染即可产生高滴度病毒载体,制作工艺更简化,成本更低,可以更好地控制产品质量并进行大规模的生产;相较于能够稳定包装的GALV逆转录病毒,可以在较低MOI下实现NK细胞、T细胞等难转导的原代免疫细胞的高效转导,转导阳性率大幅度提高的同时还能维持稳定,且不影响免疫细胞的活率与扩增。

END


微信公众号


市场部:赖女士
了解更多内容请登录
www.sz-cell.com
全国统一服务热线
400-800-1266
 扫一扫,关注我们最新消息
扫一扫,关注我们最新消息 工作时间:周一至周五 9:00-18:00
联系人:赖女士
手机:13670105633
邮件:laijiaqi@sz-cell.com
地址:深圳市坪山区坑梓街道金沙社区荣田路1号海普瑞生物医药生态园
